Semaglutida 50 mg oral diária para tratamento de adultos com sobrepeso ou obesidade – estudo OASIS 1
TERAPIA FARMACOLÓGICA - OBESIDADE
7/1/20235 min read


Por Rossella Dias


A semaglutida é um análogo do hormônio glucagon-like peptide-1 (GLP-1) disponível atualmente nas formulações subcutânea (semanal) e oral (diária). Já sabemos que a semaglutida subcutânea na dose de 2,4 mg semanal foi aprovada para o tratamento do sobrepeso e da obesidade, com redução substancial do peso e melhora de fatores de risco cardiovasculares em pacientes com ou sem diabetes mellitus tipo 2 (DM2), baseado nos achados dos estudos do programa STEP. Também foi aprovada a semaglutida oral nas doses de 7mg e 14mg para o tratamento do DM2. Agora, uma dose maior da semaglutida oral (50 mg) foi estudada para o tratamento de pacientes com sobrepeso e obesidade.
Recentemente, no congresso da American Diabetes Association, foi apresentado o estudo OASIS 1, cujo objetivo foi avaliar a eficácia e a segurança da semaglutida oral na dose diária de 50 mg para o tratamento do sobrepeso ou obesidade em adultos sem DM2, associada a intervenções em estilo de vida.
Trata-se de um um ensaio clínico de superioridade, fase 3, randomizado, duplo-cego, placebo controlado, multicêntrico, que comparou a semaglutida oral 50mg versus placebo (pareado 1:1) durante 68 semanas de tratamento (e por mais 7 semanas após, sem tratamento). Os critérios de inclusão foram: idade >= 18 anos (>=20 anos para japoneses, devido requisitos regulatórios do país), IMC >= 30kg/m² ou IMC >=27Kg/m² com uma ou mais complicações ou comorbidades associadas ao peso (HAS, DLP, SAOS ou doença cardiovascular). Foram excluídos candidatos que apresentaram perda de mais de 5kg de peso nos 3 meses anteriores ao screening, cirurgia bariátrica prévia (ou planejada), HbA1C >= 6,5% ou história de DM tipo 1 ou 2. A semaglutida oral era iniciada em 3 mg, com escalonamento da dose a cada 4 semanas (ou mais, se necessário, para melhorar a tolerabilidade) para 7 mg, 14 mg, 25 mg, até 50 mg (dose de manutenção).
Os desfechos primários avaliados foram: porcentagem de perda de peso até a 68ª semana e ocorrência de pelo menos 5% de perda de peso até a 68ª semana. Os desfechos secundários foram: redução de pelo menos 10%, 15% e 20% do peso até a 68ª semana, e avaliação de mudança dos resultados de função física auto-relatada pelos participantes. A avaliação da segurança abordou o número de eventos adversos até a 75ª semana.
Quais foram os resultados?
Entre setembro a novembro de 2021, 667 participantes foram selecionados e randomizados entre os dois grupos: semaglutida oral 50mg (n=334) ou placebo (n=333). A média de idade foi de 50 anos, peso corporal de 105,4kg, IMC médio inicial de 37,5Kg/m² e circunferência abdominal de 113,6cm. A maioria dos participantes era do gênero feminino (73%) e brancos (74%). 613 participantes tinham um IMC inicial de pelo menos 30kg/m² e 54 tinham IMC >= 27kg/m² porém < 30kg/m², associado a complicações/comorbidades.
A maioria dos participantes completou o tratamento (até a 68ª semana): 86% no grupo da semaglutida e 78% no grupo placebo. Dentre os que completaram o tempo de tratamento, 80% dos participantes do grupo semaglutida estavam na dose de 50mg na 68ª semana.
A média de perda de peso até a 68ª semana foi de 15,1% no grupo semaglutida versus 2,4% no grupo placebo. Na análise de dados correspondentes considerando o tratamento sendo realizado como pretendido (ou seja, excluindo interrupções temporárias), a perda de peso foi de 17,4% no grupo semaglutida versus 1,8% no grupo placebo. O número de participantes que atingiram pelo menos 5% de perda de peso até a 68ª semana foi de 85% no grupo semaglutida versus 26% no grupo placebo – ou seja, o número de participantes que atingiu essa porcentagem de perda de peso foi pelo menos 3 vezes maior no grupo semaglutida.
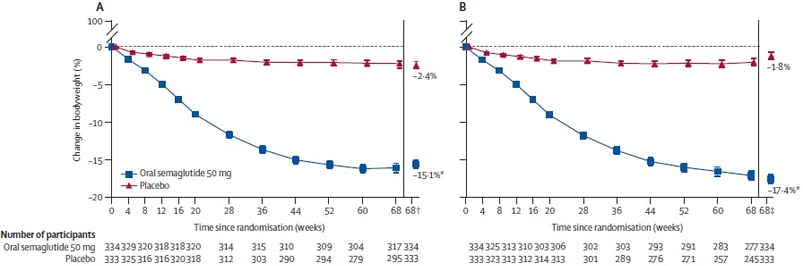

Figura 1: Variações percentuais médias do peso até a 68ª semana de tratamento. (A: análise independentemente da descontinuação do produto do ensaio ou de outras terapias redutoras de peso - “treatment policy estimand” / B: análise excluindo interrupções e sem intervenções de resgate - “trial product estimand”)
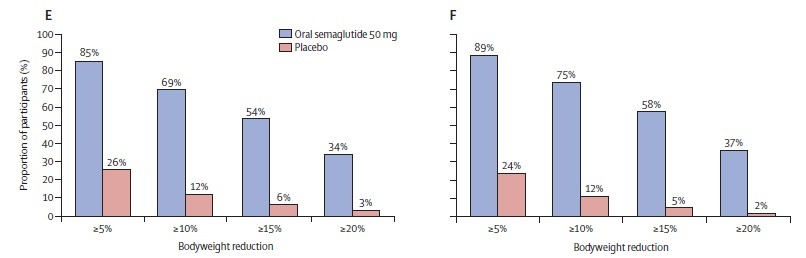
Figura 2: Proporções dos participantes que atingiram pelo menos 5%, 10%, 15% e 10% de perda de peso. (E: “treatment policy estimand" / F: “trial product estimand”)
Além disso, uma proporção maior de participantes no grupo semaglutida atingiu redução do peso corporal de pelo menos 10%, 15% e 20% durante o período de tratamento (até a semana 68), quando comparados com o grupo placebo. No grupo semaglutida, 69% dos participantes perderam pelo menos 10% do peso até a 68ª semana, 54% perderam >= 15% e 34% perderam >= 20% do peso.
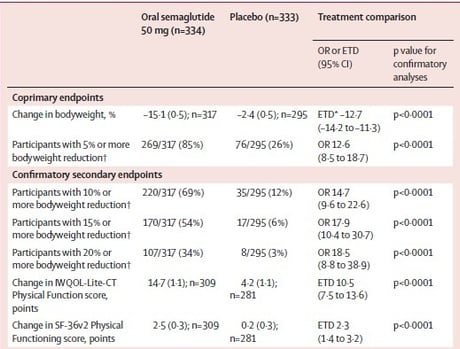
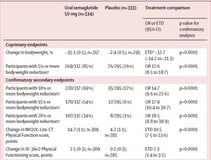
Tabela 1: Resultados dos desfechos primários e secundários.
E quanto a segurança da medicação?
Os efeitos adversos mais frequentemente relatados com a semaglutida oral 50mg foram os gastrointestinais – náusea, constipação, diarreia e vômitos. Esses efeitos colaterais eram tipicamente transitórios e de gravidade leve-moderada, e se resolviam sem a descontinuação permanente do tratamento. Eles atingiram um pico de incidência durante a fase de escalonamento da dose da medicação.
O perfil de segurança da semaglutida oral foi, em geral, compatível com a semaglutida subcutânea e com a classe de análogos do GLP1 como um todo.
Conclusão:
A semaglutida oral na dose diária de 50 mg mostrou induzir uma redução de peso substancial e clinicamente significativa quando usada em associação a intervenções em estilo de vida (dieta e atividade física). Portanto, poderia ser considerada como uma futura opção efetiva para o tratamento do sobrepeso ou obesidade.
Bibliografia:
Knop FK, Aroda VR, do Vale RD, Holst-Hansen T, Laursen PN, Rosenstock J, Rubino DM, Garvey WT; OASIS 1 Investigators. Oral semaglutide 50 mg taken once per day in adults with overweight or obesity (OASIS 1): a randomised, double-blind, placebo-controlled, phase 3 trial. Lancet. 2023 Jun 23:S0140-6736(23)01185-6.